QUÍMICA UNI PREGUNTAS RESUELTAS DE EXAMEN ADMISIÓN UNIVERSIDAD
PREGUNTA 1 :
Una de las preocupaciones a nivel mundial es el calentamiento global originado por las actividades del hombre.
Al respecto, señale la alternativa que presenta la secuencia correcta después de determinar si las proposiciones son verdaderas (V) o falsas (F).
I) El calentamiento global es consecuencia del aumento de la temperatura en la atmósfera terrestre.
II) El cambio climático que ocurre en la Tierra está relacionado principalmente al impacto de los gases de efecto invernadero.
III) El término efecto invernadero se refiere a la retención del calor en la atmósfera por parte de una capa de gases en la atmósfera, como por ejemplo el dióxido de carbono, el vapor de agua y metano.
A) VVV
B) VFV
C) VFF
D) FFV
E) FFF
RESOLUCIÓN :
El efecto invernadero es un fenómeno natural, en donde la luz solar que atraviesa la atmósfera se absorbe y calienta la superficie de la tierra. La superficie caliente emite radiación infrarroja (calor) que es absorbida por el metano, vapor de agua y CO2, principalmente, y es retenido en la atmósfera produciendo un efecto de calentamiento y como consecuencia, cambios en el clima.
Este fenómeno natural es crucial para mantener la adecuada temperatura en la tierra, sin él la tierra estaría cubierta de hielo permanentemente. Sin embargo, el contenido de estos gases en los últimos tiempos, ha incrementado considerable- mente, especialmente el CO2, debido a la combustión y a la deforestación de las zonas tropicales. Ocasionando un aumento en la temperatura media de la tierra, provocando calentamiento global.
Analizamos las proposiciones
I) Verdadera
A mayor temperatura de la atmósfera del planeta, se origina calentamiento global.
II) Verdadera
Los gases de efecto invernadero incrementan la temperatura de la Tierra.
III) Verdadera
El CO2 , CH4 y H2O retienen el calor que debió salir del planeta.
Rpta. : "A"
PREGUNTA 2 :
La eutroficación se considera como una de las causas que afecta a la vida acuática.
Al respecto, indique la secuencia correcta después de determinar si la proposición es verdadera (V) o falsa (F).
I) Es un crecimiento desmesurado de plantas acuáticas por exceso de nutrientes en el agua.
II) Se origina por la presencia de nitratos y fosfatos en cuerpos de agua de poca corriente.
III) El uso de detergentes y fertilizantes puede causar este problema.
A) FVV
B) VFV
C) FFV
D) FFF
E) VVV
RESOLUCIÓN :
CONTAMINACIÓN AMBIENTAL
La eutroficación es el crecimiento desmesurado de vegetación acuática debido al exceso de nutrientes en el agua, originada por la presencia de nitratos y fosfatos en el agua de poca corriente y que tiende a estancarse.
Los detergentes (nitratos) y fertilizantes (fosfatos) pueden causar este problema. La eutroficación constituye un proceso de envejecimiento de un lago hasta convertirse en un bosque debido al enriquecimiento de nutrientes que ocurre en un largo tiempo (cientos de años).
La descarga de desechos sólidos, aguas negras sin tratar (contienen detergentes, desechos fecales) y de residuos agrícolas que llegan a un lago o río acelera el envejecimiento y su conversión a un bosque.
Analizamos las proposiciones.
I) Verdadera
Debido a la eutroficación, las plantas acuáticas se desarrollan por efecto del exceso de nutrientes que llegan a través de los ríos.
II) Verdadera
Los nitratos y fosfatos al llegar a los lagos (agua de poca corriente) causan la eutroficación.
III) Verdadera
Los detergentes y fertilizantes contienen nutrientes y causan la eutroficación.
Rpta. : "E"
PREGUNTA 3 :
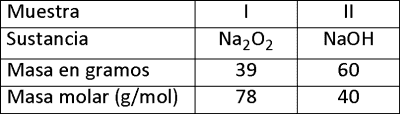
Dada la siguiente información:
Señale la alternativa correcta.
A) La muestra I corresponde a 1,5 mol de Na2O2
B) La muestra II corresponde a 0,5 mol de NaOH.
C) Ambas muestras presentan igual número de moles.
D) La muestra I presenta mayor número de moles que la muestra II.
E) La muestra II presenta mayor número de moles que la muestra I.
RESOLUCIÓN :
PREGUNTA 4 :
Los elementos del grupo 17 de la tabla periódica moderna son conocidos como halógenos (“formadores de sales”).
¿Cuál de los siguientes compuestos corresponde a una sal de un halógeno?
A) NH4NO3
B) K2S
C) NaCℓ
D) Mg3N2
E) Br2
RESOLUCIÓN :
Los elementos del grupo 17 o VIIA son conocidos como halógenos (F, Cℓ, Br, I) porque tienen la capacidad para formar sales.
Analizamos las alternativas propuestas.
A) No corresponde.
El NH4NO3 es un oxisal que no contiene un halógeno.
B) No corresponde
El K2S es una sal haloidea, pero no contiene un halógeno.
C) Sí corresponde
El NaCℓ es una sal que contiene al cloro, que es un halógeno.
D) No corresponde
El Mg3N2 es una sal haloidea que no contiene un halógeno.
E) No corresponde
El Br2 es una sustancia simple.
Rpta. : "C"
PREGUNTA 5 :
Respecto al recurso agua, ¿cuáles de las siguientes proposiciones son correctas?
I) El agua nunca se encuentra pura en la naturaleza, debido a la facultad que tiene para disolver o dispersar diferentes sustancias.
II) El agua de lluvia recolectada, en la azotea de una vivienda, en un recipiente esterilizado, es agua pura.
III) La contaminación de las aguas con materia orgánica biodegradable disminuye la concentración de oxígeno disuelto.
A) solo I
B) solo II
C) solo III
D) I y III
E) I, II y III
RESOLUCIÓN :
CONTAMINACIÓN AMBIENTAL
I) El agua nunca se encuentra pura en la naturaleza, debido a la facultad que tiene para disolver o dispersar diferentes sustancias.
Correcta, el agua se encuentra en la naturaleza formando los océanos, mares, ríos, etc.
II) El agua de lluvia recolectada en la azotea de una vivienda, en un recipiente esterilizado, es agua pura.
Incorrecta, el agua de lluvia es una mezcla, cuyo pH es ácida, debido a la presencia de ácido nítrico, ácido sulfúrico y ácido sulfuroso, que se forman al reaccionar, el agua (presente en la humedad del aire) con óxido de nitrógeno, dióxido de azufre y trióxido de azufre, los cuales son emitidos por las fábricas, vehículos, etc.
III) La contaminación de las aguas con materia orgánica biodegradable disminuye la concentración de oxígeno disuelto.
Correcta, la disminución de oxígeno ocurre al momento del proceso de degradación de la materia biodegradable.
Rpta. : "D"
PREGUNTA 6 :
Respecto a la teoría mecano-cuántica y la estructura atómica, ¿cuáles de las siguientes proposiciones son correctas?
I) El electrón ya no están en una órbita, en el sentido de Bohr, sino más bien hay una nube de probabilidad electrónica.
II) Cada uno de los estados cuánticos, diferenciados por n, ℓ, mℓ, corresponde a distintas funciones de distribución de probabilidad (orbitales).
III) La función de probabilidad más sencilla se obtiene para los estado s (ℓ=10) y tienen simetría esférica.
A) solo I
B) solo III
C) I y II
D) II y III
E) I, II y III
RESOLUCIÓN :
Modelo atómico del átomo
I) El electrón ya no está en una órbita, en el sentido de Bohr, sino más bien hay una nube de probabilidad electrónica.
Afirmación correcta.
II) Cada uno de los estados cuánticos diferenciados por n, ℓ, mℓ, corresponde a distintas funciones de distribución de probabilidad (orbitales).
Afirmación correcta.
III) La función de probabilidad más sencilla se obtiene para los estados s (ℓ=0) y tienen simetría esférica.
Afirmación correcta.
Rpta. : "E"
PREGUNTA 7 :
Las propiedades de la materia se pueden clasificar en físicas y químicas. En las primeras no es necesario alterar la composición de la muestra para ser observadas, mientras que en las segundas sí lo es. Indique la secuencia correcta después de determinar si la proposición es verdadera (V) o falsa (F).
I) Las propiedades físicas son cualidades que pueden ser medidas cuando ocurre un cambio físico.
II) Son ejemplos de propiedades químicas la inflamabilidad y la corrosividad.
III) La propiedad relacionada con la reacción violenta del sodio en agua se denomina reactividad.
A) VFV
B) VFF
C) FVF
D) FFF
E) VVV
RESOLUCIÓN :
MATERIA: PROPIEDADES
I) Verdadera
Las propiedades físicas son cualidades que al ser observadas o medidas no alteran su composición. Tenemos densidad, estado físico, temperatura.
II) Verdadera
Las propiedades químicas son cualidades que al ser observadas alteran la estructura interna y forman nuevas sustancias. Tenemos inflamabilidad, corrosividad, toxicidad.
III) Verdadera
Los metales alcalinos (IA) reaccionan vigorosamente con el agua, liberando luz y se verifica su reactividad.
Rpta. : "E"
PREGUNTA 8 :
La corrosión de un metal es un proceso espontáneo a temperatura ambiente.
Al respecto, ¿cuáles de las siguientes proposiciones son correctas?
I) La corrosión implica un proceso de oxidación reducción.
II) En algunos casos, la corrosión del metal forma una capa protectora que disminuye el proceso de corrosión.
III) El daño estructural por efectos de la corrosión tiene una alta repercusión económica.
A) solo I
B) I y III
C) solo III
D) I y II
E) I, II y III
RESOLUCIÓN :
Electroquímica
La corrosión se define como el deterioro de un material a consecuencia de un ataque electroquímico por parte de su entorno. De manera más general, puede entenderse como la tendencia general que tienen los materiales a buscar su forma más estable.
La velocidad a la que tiene lugar la corrosión dependerá en alguna medida de la temperatura y la salinidad, y de la concentración del fluido en contacto con el metal.
Analizaremos cada afirmación
I) La corrosión implica un proceso de óxido- reducción.
Es correcto, la corrosión es un proceso redox, por el cual los metales se oxidan con O2 en presencia de humedad.
II) En algunos casos, la corrosión del metal forma una capa protectora que disminuye el proceso de corrosión.
Es correcta, existen varios métodos para proteger metales en contra de la corrosión y uno de ellos es hacer que forme de manera natural una película protectora, tal como óxido metálico, sobre la superficie del metal.
III) El daño estructural por efectos de la corrosión tiene una alta repercusión económica.
Es correcta, a la corrosión se debe la pérdida anual de mucho dinero en productos metálicos.
Rpta. : "E"
PREGUNTA 9 :
La notación de Lewis es la representación de los electrones de valencia de un átomo. Para los elementos 17X, 33Y y 13Z, halle sus configuraciones electrónicas y notaciones de Lewis correspondientes: Indique la respuesta correcta según la notación de Lewis.
A) solo II
B) II y III
C) solo I
D) I y III
E) I y II
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 11 :
A) 20
B) 38
C) 65
D) 80
E) 90
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 12 :
A continuación se presenta un diagrama de fases genérico. ¿En qué puntos, de los señalados, se observarán 2 fases?
A) I, III y V
B) II y IV
C) III y V
D) I y IV
E) I y III
RESOLUCIÓN :
Un diagrama de fase, es una representación gráfica de las condiciones de temperatura y presión a las que existen los sólidos, líquidos y gases, como fases únicas de los estados de la materia o como dos o más fases en equilibrio.
Las diferentes regiones del diagrama corresponde a una sola fase o estado de la materia. Las líneas curvas o rectas donde se juntan las regiones de una sola fase, representan dos fases en equilibrio. En dicho diagrama existe un punto, denominado el punto triple, en donde coexisten el estado sólido, líquido y gaseoso. Asimismo, podemos mencionar que la curva que separa las fases vapor-líquido termina en un punto denominado punto crítico.
Rpta. : "A"
PREGUNTA 13 :
¿Cuál(es) de los siguientes contaminantes primarios son causantes de la lluvia ácida?
I) CO
II) CO2
III) NOx
IV) SOx
A) III y IV
B) II y IV
C) I y II
D) solo IV
E) II y III
RESOLUCIÓN :
CONTAMINACIÓN AMBIENTAL
La lluvia ácida es aquella que posee los ácidos nítrico y sulfúrico (HNO3 y H2SO4) que se originan a partir de la emisión de los óxidos NOx y SOx que provienen de la tostación de minerales y la combustión de combustibles fósiles.
NOx+H2O → HNO3
SOx+H2O → H2SO4
Consecuencias:
• Acidificación del suelo y agua (ríos, lagos), afectando la vida acuática.
• Corrosión de metales y disolución de piedra caliza (mármol).
Rpta. : "A"
PREGUNTA 14 :
¿Cuántos de los siguientes fenómenos presentados en las proposiciones son químicos?
I) Laminación del cobre
II) Oxidación del hierro
III) Evaporación del agua
IV) Fermentación de la uva
V) Disolución del azúcar en agua
A) 1
B) 2
C) 3
D) 4
E) 5
RESOLUCIÓN :
Un fenómeno químico, es un proceso por la cual la materia se transforma, perdiendo sus propiedades físicas y química, es decir, pierde sus propiedades, y origina nuevas sustancias con propiedades diferentes a las que dieron origen.
Considerando esta premisa, analizaremos cada proposición:
I) LAMINACIÓN DEL COBRE
En el proceso de laminación del cobre, lo que se hace es reducir el espesor del cobre, manteniendo intacto las propiedades químicas, por lo tanto, no se trata de un fenómeno químico.
II) OXIDACIÓN DEL HIERRO
La oxidación es una reacción por la cual el hierro se convierte en un óxido (Fe2O3), transformándose en otra sustancia, por lo tanto, se trata de un fenómeno químico.
III) VAPORACIÓN DEL AGUA
La evaporación de agua es un fenómeno por el cual el agua sólo cambia de estado, por lo tanto no se trata de un fenómeno químico.
IV) FERMENTACIÓN DE LA UVA
En la fermentación de la uva ocurre reacciones en la que se producen sustancias como el etanol y el dióxido de carbono, por lo tanto, se trata de un fenómeno quí- mico.
V) DISOLUCIÓN DE AZÚCAR EN AGUA
El azúcar disuelta en agua no pierde sus propiedades, al igual que el agua, se les puede separar por procesos físicos sin que pierda sus propiedades originales, por lo tanto, no es un fenómeno químico.
Finalmente, son fenómenos químicos II y IV
Rpta. : "B"
PREGUNTA 15 :
Dados los siguientes procesos:
Indique la proposición correcta:
A) La primera energía de ionización del cloro corresponde a un proceso exotérmico.
B) La segunda energía de ionización del cloro es menor que la primera.
C) Es más fácil que el cloro pierda electrones que los gane.
D) La primera afinidad electrónica del cloro corresponde a un fenómeno endotérmico.
E) El ion Cℓ(g)– es más estable que el átomo de Cℓ(g).
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 16 :
¿Cuál (es) de los siguientes esquemas representan a una sustancia?
A) solo II
B) I, II y III
C) I y III
D) II y IV
E) solo I
RESOLUCIÓN :
Rpta. : "C"
PREGUNTA 17 :
La sanguina seca (pintura roja) contiene, como pigmento, aproximadamente el 63% en masa de óxido férrico, ¿cuántos mililitros de ácido clorhídrico 2M se requieren para que todo el pigmento contenido en 10 g de sanguina reacciones totalmente con el ácido?
A) 20
B) 40
C) 79
D) 118
E) 137
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 18 :
La determinación de la concentración de peróxido de hidrógeno, H2O2 , en el agua oxigenada, puede llevarse a cabo mediante la titulación denominada permanganometría, de acuerdo con la siguiente ecuación química:
Al respecto, ¿cuáles de las siguientes proposiciones son correctas?
I) El H2O2 actúa como agente oxidante en esta reacción.
II) Si una muestra de 25 mL de agua oxigenada consume 15 mL de KMnO4 (0,01 M), dicha muestra contiene 3,25×10–4 moles H2O2
III) Dentro del material necesario para realizar esta operación se encuentra una bureta.
A) solo II
B) I, II y III
C) solo III
D) I y III
E) solo I
RESOLUCIÓN :
Rpta. : "C"
PREGUNTA 19 :
En el horno eléctrico de una siderúrgica se coloca chatarra de acero y después de unos minutos se observa la formación de gases pardo-rojizos los cuales, en corto tiempo, se difunden en el área de trabajo y la zona aledaña. Por otro lado, el acero fundido obtenido en el horno, se vierte en moldes de madera. Pasado un tiempo, a partir del acero fundido se obtienen bolas de acero utilizadas en los molinos. ¿Cuántas de las observaciones subrayadas involucran cambios físicos y químicos, respectivamente?
A) 0, 4
B) 1, 3
C) 2, 2
D) 3, 1
E) 4, 0
RESOLUCIÓN :
MATERIA
Se pide reconocer si los cambios son a nivel físico o químico, lo que ocurre en el horno eléctrico de una siderurgia, donde se procesa una chatarra de acero (hierro oxidado).
Recordemos que la materia se encuentra en permanente cambio. Si el cambio es a nivel físico (la materia mantiene su composición), así como si el cambio es a nivel químico (la materia cambia su composición química). Entonces analizamos las observaciones subrayadas:
• Formación de gases pardo-rojizo: cambio químico
• Se difunden en el área de trabajo: cambio físico
• El acero fundido obtenido en el horno: cambio físico
• A partir del acero fundido se obtienen bolas de acero utilizadas en los molinos: cambio físico
Entonces hay tres cambios físicos y un cambio químico.
I) La formación de gases pardo-rojizos implica la aparición del NO2 que se forma a partir del N2 atmosférico por la alta temperatura en el horno (cambio químico).
II) La difusión del NO2 implica un cambio físico.
III) El acero fundido implica un cambio físico de sólido a líquido.
IV) Del acero fundido se obtiene bolas de acero, implica otro cambio físico de líquido a sólido.
Rpta. : "D"
PREGUNTA 20 :
Los polímeros son grandes moléculas constituidas por una unidad fundamental (monómero) que se repite.
Respecto a los tipos de polímeros, y siendo A y B dos monómeros, indique la relación correcta .
I) Homopolímero
II) Copolímero
III) En bloque
a) ~A – B – A – B – A – B ~
b) ~A – A – A – A – A – A ~
c) ~A – A – A – B – B – B ~
A) Ia, IIb, IIIc
B) Ic, IIb, IIIa
C) Ia, IIc, IIIb
D) Ib, IIc, IIIa
E) Ib, IIa, IIIc
RESOLUCIÓN :
POLÍMEROS
Los polímeros son macromoléculas formadas por unión mediante enlaces covalentes de uno o más tipos de unidades simples llamadas monómeros. Pueden clasificarse según su cadena como
Rpta. : "E"
PREGUNTA 21 :
¿Cuántos gramos de sulfato de cobre pentahidrato, CuSO4·5H2O, serán necesarios para preparar 250 mL de una solución 0,1 M de CuSO4?
Masa atómica: Cu=63,5; S=32; O=16; H=1
A) 3,99
B) 5,12
C) 6,24
D) 8,75
E) 10,23
RESOLUCIÓN :
Rpta. : "C"
PREGUNTA 23 :
Los sistemas dispersos se pueden clasificar de acuerdo con el tamaño de partícula de su fase dispersa en suspensión, coloide y solución.
Respecto a los sistemas dispersos, señale la secuencia correcta después de determinar si la proposición es verdadera (V) o falsa (F).
I) El tamaño de la partícula dispersa en un coloide es mayor que la de una suspensión.
II) La fase dispersa en una suspensión se puede separar por filtración.
III) Los componentes de una solución pueden sedimentar por acción a la gravedad.
A) FVF
B) FFF
C) FVV
D) VFV
E) VVV
RESOLUCIÓN :
SISTEMAS DISPERSOS
Los sistemas dispersos son mezclas de dos o más sustancias simples o compuestas, en donde existe una fase dispersa o discontinua y una dispersante o continua.
I) El tamaño de la partícula dispersa en un coloide es menor que la de una suspensión.
II) El tamaño de las partícula de una suspensión permite separarlo por filtración.
III) Las partículas de la fase dispersa en una solución están en el orden atómico y molecular razón por la cual no pueden sedimentar.
Rpta. : "A"
PREGUNTA 24 :
Una posible solución a la contaminación relacionada a los gases emanados por los motores de los autos es el uso de celdas de combustible H2-O2.
Al respecto, ¿cuáles de las siguientes proposiciones son correctas?
I) En la celda se producen reacciones de oxidación-reducción.
II) La celda produce agua como producto.
III) La celda produce principalmente energía térmica.
A) I y II
B) I y III
C) II y III
D) solo II
E) solo III
RESOLUCIÓN :
La celda de combustible es un dispositivo que produce electricidad y agua, mediante un proceso inverso a la electrólisis.
Esta celda esta constituida por dos electrodos (ánodo y cátodo), un electrolito, H2 (combustible) y O2 (oxidante).
En el ánodo se produce la reacción de oxidación del combustible, generando electrones y protones, mientras que en el cátodo se produce la reacción de reducción del oxígeno.
Analizamos las proposiciones.
I) Correcta
Se producen dos reacciones:
• oxidación del hidrógeno (combustible)
• reducción del oxígeno (comburente)
II) Correcta
El H2O es el único producto.
III) Incorrecta
La principal energía liberada es la eléctrica.
Rpta. : "A"
PREGUNTA 25 :
Respecto a los sistemas dispersos que pueden producirse en sistemas químicos, indique la secuencia correcta luego de confirmar si las proposiciones son verdaderas (V) o falsas (F):
I) Las suspensiones no se sedimentan.
II) Las soluciones no dispersan la luz.
III) Los coloides dispersan la luz.
A) FVV
B) VVV
C) FFF
D) VFF
E) VVF
RESOLUCIÓN :
Los sistemas dispersos (mezclas) se clasifican según el tamaño de las partículas dispersas y de ciertas características: en suspensión, coloide y solución.
I. Falsa
Las suspensiones al reposar las partículas dispersas (tamaño mayor a 1000 nm) sedimentan por acción de la gravedad.
II. Verdadera
Las soluciones cuyas partículas dispersas son átomos, iones, moléculas (tamaño menor a 1 nm) no permiten la dispersión de la luz.
III. Verdadera
Los coloides (partícula coloidal), cuyo tamaño está comprendido entre 1 nm a 1000 nm, estas dispersan la luz (efecto Tyndall).
Rpta. : "A"
PREGUNTA 26 :
Respecto al 3-metil-1-butino, ¿cuáles de las siguientes proposiciones son correctas?
I) Tiene 11 enlaces sigma (σ).
II) Presenta 3 enlaces pi (𝛑).
III) No presenta isomería geométrica.
A) I y II
B) II y III
C) solo I
D) solo II
E) solo III
RESOLUCIÓN :
Analizamos cada proposición.
I) Incorrecta
La molécula presenta 12 enlaces sigma
II) Incorrecta
La molécula presenta 2 enlaces pi
III) Correcta
Isomería geométrica no es característica de los alquinos, sino de los alquenos y cicloalcanos.
Rpta. : "E"
PREGUNTA 27 :
Durante el fenómeno de la disolución pueden desarrollarse una serie de interacciones intermoleculares. ¿Cuáles de las siguientes son posibles?
I) Puente de hidrógeno
II) Ion-dipolo
lll) Dipolo-dipolo inducido
A) solo I
B) solo II
C) solo III
D) I y II
E) I, II y III
RESOLUCIÓN :
FUERZA INTERMOLECULARES
Durante el fenómeno de disolución se producen interacciones entre las moléculas y/o iones del soluto y las moléculas del solvente.
☛ Puente hidrógeno
☛ Ion - dipolo permanente
☛ Ion - dipolo inducido
☛ Dipolo permanente - dipolo permanente
☛ Dipolo permanente - dipolo inducido
☛ Dipolo instantáneo - dipolo inducido
Rpta. : "E"
PREGUNTA 28 :
PREGUNTA 29 :
Una solución preparada mezclando 5g de tolueno, C7H8, con 225 g de benceno, C6H6, tiene una densidad de 0,976 g/mL. Calcule la molaridad del tolueno en dicha solución.
Masas molares (g/mol): tolueno=92; benceno=78
A) 0,05
B) 0,11
C) 0,15
D) 0,23
E) 0,26
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 30 :
¿Cuál o cuáles de los siguientes esquemas del ion nitrito, NO2– representa la estructura de Lewis correcta?
Dato, Número atómico: N=7, O=8
A) solo III
B) solo I
C) I y III
D) I y IV
E) II y IV
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 31 :
La polaridad de una sustancia depende si su molécula es polar o apolar.
En las proposiciones que se mencionan, señale la combinación correcta después de determinar si la proposición es verdadera (V) o falsa (F).
I) La molécula del sulfuro de hidrógeno (H2S) es polar.
II) La molécula de la fosfina (PH3) es no polar.
III) La unidad fórmula del bromuro de sodio (NaBr) es polar.
A) VFF
B) FVV
C) VVF
D) VVV
E) FFV
RESOLUCIÓN :
Rpta. : "A"